Nature:艾沐蒽助力吸入式疫苗开发,直达肺泡,有效沉积
发布时间:2024-01-11 15:29 | 点击次数:803

研究背景
COVID-19是由SARS-CoV-2引起的一种严重急性呼吸系统综合症,于2020年被宣布为大流行。疫苗接种是成功预防和控制该疾病传播的公共卫生干预措施。迄今为止,已批准多种类型的SARS-CoV-2疫苗,包括灭活疫苗、蛋白亚单位疫苗、mRNA疫苗和病毒载体疫苗。这些疫苗大多通过肌肉注射给药,诱导产生血清学IgG,从而中和病毒的传染性并缓解COVID-19的症状。然而,由于肌肉注射疫苗无法在气道粘膜组织中诱导免疫反应,而正是这些组织是SARS-CoV-2进入的部位,因此在分泌型IgA和IgG方面存在不足。此外,目前的COVID-19疫苗需要在低温“冷链”条件下制造、运输、储存和管理,增加了成本。
研究结果
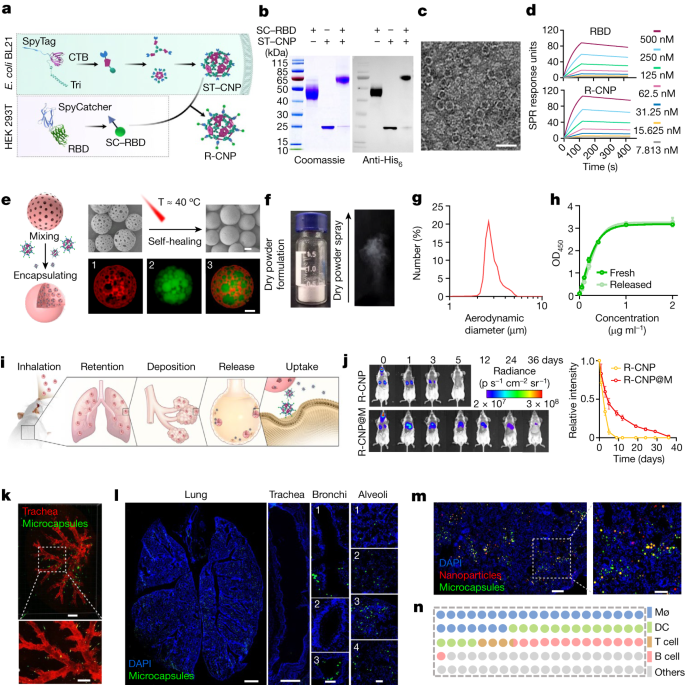
考虑到直接吸入纳米级制剂在肺泡中的沉积能力较差,并且先前的研究已经报道了空气动力学直径在1-4µm范围内的颗粒在肺泡中的有效输送,作者通过将R-CNPs放置在合适的空气动力学尺寸的微胶囊中进行R-CNP@M设计。这应该允许有效地递送到肺泡,并使R-CNPs持续释放,以支持持续的抗原刺激。作者采用膜乳化方法制备多孔PLGA微球,通过简单混合和温和的加热介导密封R-CNPs(图1e)通过微调膜孔径、渗透梯度和孔隙演化时间,可以控制微球的粒径、孔隙度和空腔容积,从而优化R-CNP@M获得合适的气动尺寸和较高的封装效率。使用共聚焦激光扫描显微镜对所得R-CNP@M进行了表征,三维重建提供了强有力的证据,证明尼罗河红标记微胶囊的内腔充满了异硫氰酸荧光素(FITC)标记的R-CNPs(图1e)。R-CNP@M经冻干后呈白色粉末状,分散性极好,用干粉气溶胶发生器(DPAG)喷射后可形成均匀的雾(图1f)。这些冻干的微胶囊几乎完全在理想的空气动力学尺寸范围内(2-4µm;图1 g)。此外,他们显示R-CNP在五周内持续释放,并且释放的R-CNP与新鲜的R-CNP对hACE2的结合亲和力没有差异(图1h)。存储一个月后的测试表明,R-CNP@M的气动直径和封装后的R-CNP的水动力直径变化可以忽略不计,支持良好的存储稳定性。
3.体内生物分布和释放
作者研究了干粉吸入器(DPI)给药后其在肺部的保留、沉积、释放和摄取情况(图1i)。为了测量保留率,作者提供了含有cy7标记的R-CNPs的微胶囊疫苗,并纳入了一组接受等效cy7标记的R-CNPs气溶胶给药的小鼠进行比较(图1j)。与R-CNP组小鼠5天后肺部无荧光信号相比,R-CNP@M组小鼠第5天肺部仍有50%的初始信号强度,直到第42天仍有荧光信号。与R-CNP相比,R-CNP@M的曲线下面积值提高了3.5倍,表明R-CNP@M可以在肺中诱导持续的抗原刺激。
作者用链霉亲和素- AF647和尼罗红分别标记气管和微胶囊,并用薄层显微镜检查其分布。以吸入后第5天右上肺叶为例,微胶囊均匀分布于肺叶(图1k)。全肺组织切片(第5天)显示,气管、原发性支气管和继发性支气管中微胶囊较少,大多数微胶囊沉积在远端肺,包括末端支气管和肺泡(图1l和扩展数据图3h)。第10天的切片显示来自R-CNPs和微球的非共定位信号,支持R-CNPs从降解的微胶囊中成功释放(图1m)。流式细胞术证实了肺中APCs对这些R-CNPs的有利摄取,近一半的APCs存在于R-CNP阳性细胞中(图1n)。这些结果表明,R-CNP@M疫苗可以有效地递送到肺泡,并且微胶囊释放的R-CNPs被APC内化。
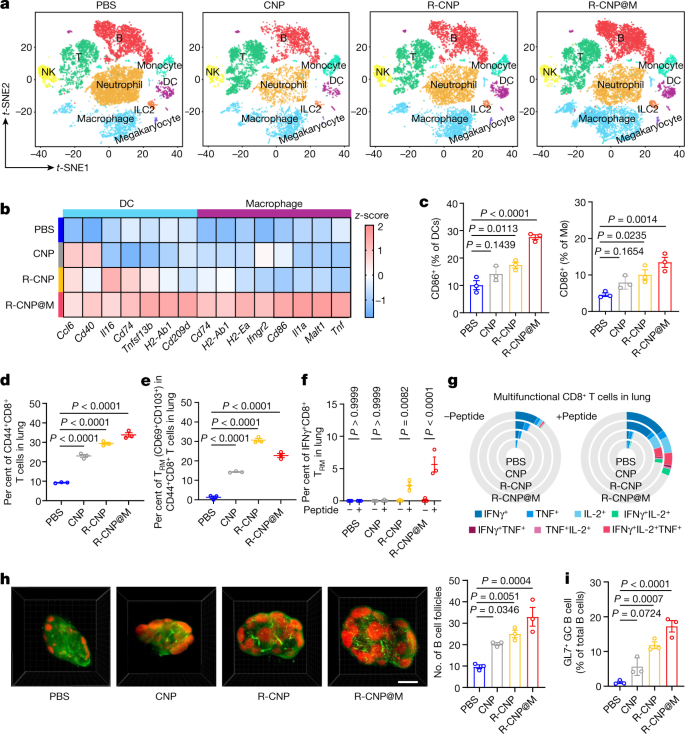
为了研究吸入疫苗对肺部免疫反应的影响,作者在第 21 天对肺部分免疫细胞进行了单细胞 RNA 测序(scRNA-seq)。scRNA-seq 数据分为九种细胞类型(图 2a),以 APC(树突状细胞和巨噬细胞)为重点,接种组的比例和数量均有所增加。作者还评估了呼吸道中的 T 细胞反应,在下呼吸道,免疫后 21 天和 70 天 CD8+ 记忆 T 细胞的比例依次为 PBS、CNP、R-CNP 和 R-CNP@M(图 2d)。到第 70 天,R-CNP 组 CD8+ 组织驻留记忆 T(TRM)细胞的比例从第 21 天的 30.63 ± 1.24% 降至 11.06 ± 2.81%,而 R-CNP@M 组在两个取样日的比例均保持在 21% 左右,这表明持续释放有利于 CD8+ TRM 细胞的长期维持(图 2e)。
作者分别鉴定CD8+和CD4+ T细胞的RBD表位(CGPKKSTNL和VGGNYNYLYRLFRKS),能够研究表位特异性T细胞反应。在下呼吸道,R-CNP@M组在分泌IFN-γ的TRM细胞反应的幅度和持续时间上都优于其他组(图2f)。作者还评估了细胞内细胞因子(IFNγ, TNF和白细胞介素(IL)-2)来评估肺中CD8+ T细胞的多功能性,R-CNP@M组在表位刺激下显示双阳性和三阳性CD8+ T细胞的比例显着增加(图2g)。接下来还评估了主要介导体液免疫的B细胞反应。光片成像显示B细胞卵泡明显增大(按PBS、CNP、R-CNP和R-CNP@M的顺序增大),提示后两组诱导了含有生发中心(GCs)的次级卵泡(图2h)。此外,通过流式细胞术检测到的生发中心B细胞(IgD−GL7+B220+)比例最高(图2i),以及记忆B细胞分化的基因表达显著上调,都支持了R-CNP@M诱导的有效体液反应。
作者对小鼠的抗体产生情况进行评估(图 3a)。结果显示,与两剂游离 R-CNP相比,单剂 R-CNP@M能更快、更强地提高血清中 RBD 特异性 IgM、IgG、IgG1 和 IgG2a 的抗体滴度,而 CNP 组则检测不到 RBD 特异性抗体(图 3b)。值得注意的是,在12个月的时间里,R-CNP@M的抗RBD抗体滴度保持在相对较高的水平,这可能与降解微胶囊持续供应免疫原性R-CNPs有关。通过对肺淋巴细胞B细胞受体(BCR)测序数据显示出高水平的种系分化,进一步表明这种长期抗体应答似乎有望通过加速亲和成熟来提高抗体质量(补充数据图6d-j)。
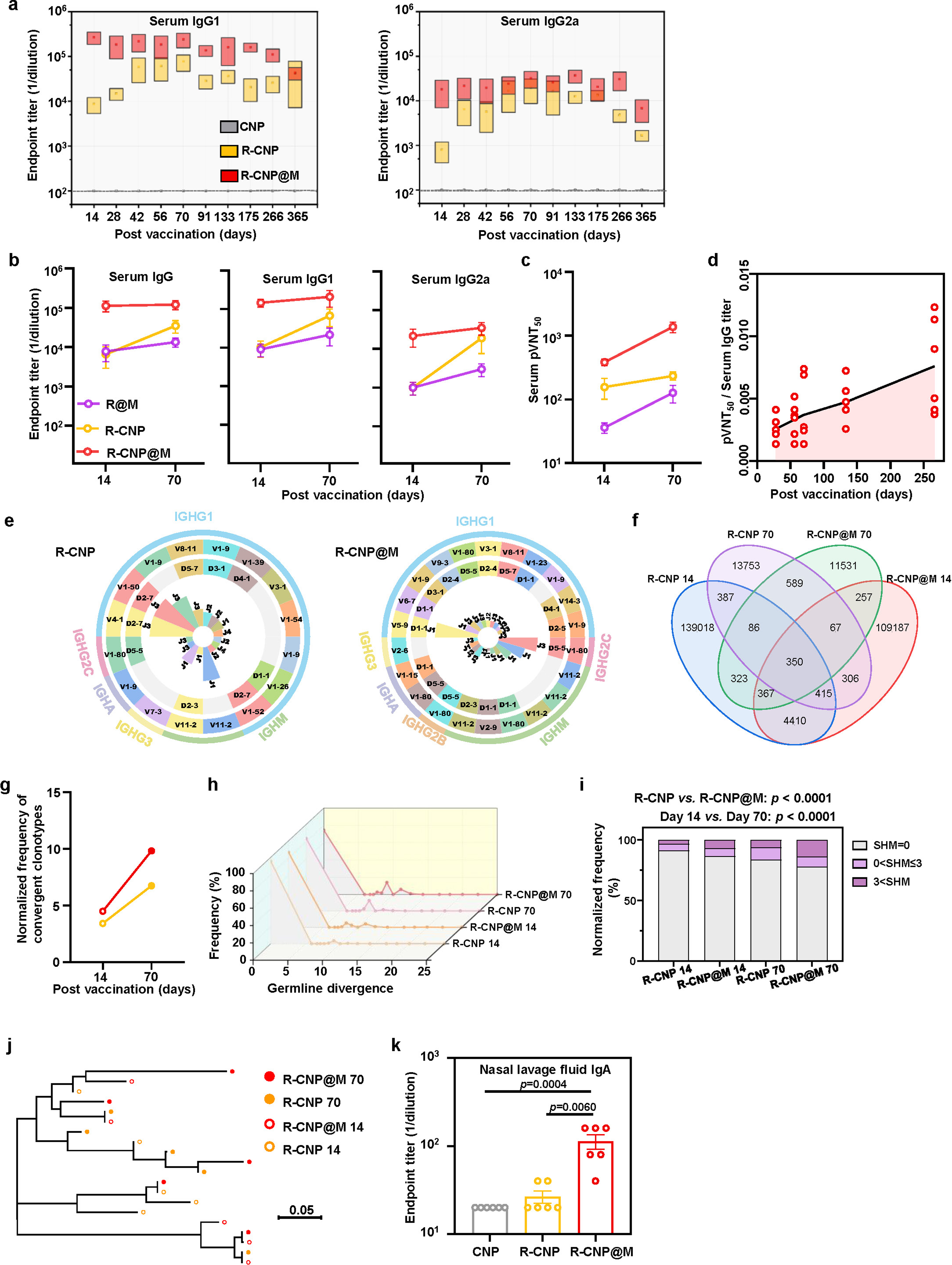
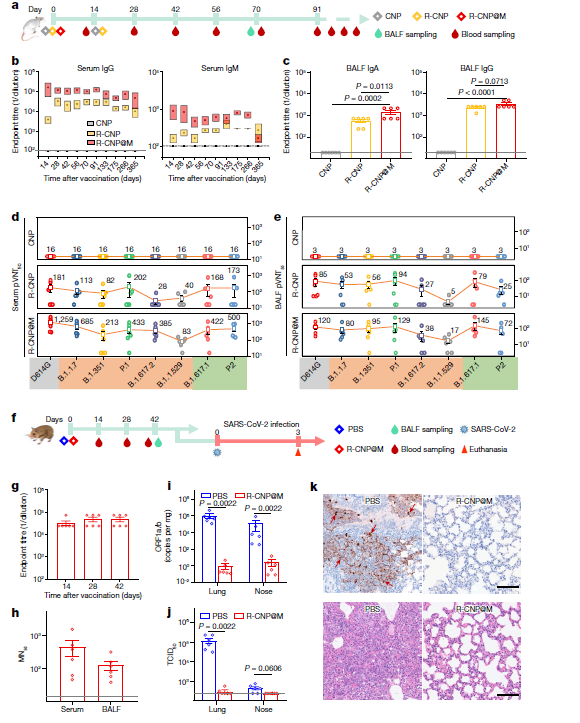
图3:小鼠和仓鼠中R-CNP@M对SARS-CoV-2的免疫学评估
为了使疫苗更接近临床,作者用非人灵长类动物进行了实验(图 4a)。一只使用尼罗河红标记疫苗的猴子在第 14 天死亡后,作者收集了它的肺部进行冷冻组织切片和成像。R-CNP@M 颗粒大部分沉积在肺泡中,只有少量微囊明显存在于气管和支气管中(图 4b,c)。在验证了疫苗在非人灵长类动物中的安全性后,作者研究了针对 SARS-CoV-2 的全身和粘膜反应。在血清学抗体反应方面,抗 RBD IgG 滴度在第 84 天仍大于 104,抗体质量高于第 14 天(图 4d,e)。关于 BALF 中的抗体反应,R-CNP@M 组也检测到了高滴度的 RBD 特异性 IgA 和 IgG(图 4f)。值得注意的是,血清和 BALF 样本对伪型病毒和活病毒都表现出良好的抵抗能力(图 4g、h),这进一步证实了 R-CNP@M 疫苗在有效抵御 SARS-CoV-2挑战方面的价值。
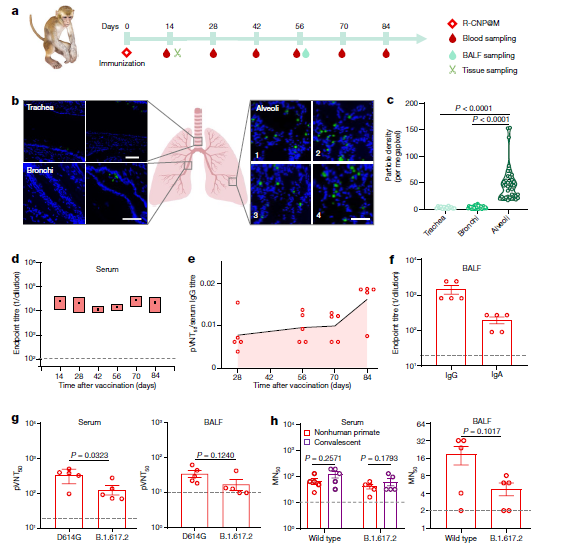
图4:R-CNP@M在食蟹猴中的表现
为了提供上述数据更清晰的可视化,作者进行了主成分分析。根据抗体反应性、样本来源、检测方法、抗体类型等数据特征,对10项免疫学指标进行降维处理后,将三组疫苗的数据清晰地划分为不同的簇(图5f)。可视化热图显示,RWT-CNP@M和RO-CNP@M疫苗显示出非常低的株不匹配免疫指标水平,而马赛克RWTRO-CNP@M疫苗的大多数免疫指标的分数显示在野生型菌株和Omicron变体都很高(图5g)值得注意的是,首次接种RWTRO-CNP@M和加强接种RWTRO-CNP@M也会导致野生型和Omicron的RBD结合效价更高。因此,antigen-CNP@M设计的马赛克迭代可以扩展抗原诱导抗体反应的广度,这应该有助于管理未来多种变体共循环的情况。
由于吸入疫苗可以在呼吸道诱导强大的免疫反应,作者探索了它对宿主-宿主传播的潜在益处。作者在多个仓鼠传播模型中测试了其抗Omicron传播的性能(图5h)。在空气传播防护模型中,作者设计了一个笼式隔板,允许气流传播,但不允许直接接触或污染物(包括饮食和床上用品)传播(图5i)。一名供体接种活的Omicron菌株,在感染后24小时将其引入笼的一侧。三名受者分别接种PBS、吸入疫苗或肌肉注射疫苗,放置在另一侧(从受感的仓鼠向下流动)。在暴露于供体24小时后,吸入疫苗组在3 dpe时肺均质液中的RNA拷贝数最低,TCID50值最低(图5j,k),病理评分最低(几乎没有肺组织病理学病变)(图5l)。
在空中传播阻断模型中,作者使用的笼与空中传播防护实验中的笼相似(图5m)。每只供体仓鼠在接种欧米克隆活菌株前分别接受吸入疫苗、肌内疫苗或PBS治疗。感染24小时后,将这些供体仓鼠引入笼分隔器的一侧,并将两只受体仓鼠(幼年仓鼠)置于感染仓鼠的下游。暴露24 h后分别饲养,3 d后死亡。暴露于接种供体的受体仓鼠鼻匀浆中的病毒载量显著降低(图5n)。值得注意的是,12名接受PBS治疗的供者中有11人感染,12名接受肌肉注射疫苗免疫的供者中有8人感染,但12名接受吸入疫苗供者中只有3人感染(图5 0,p)。这些结果支持了这样一种观点,即吸入疫苗在呼吸道中诱导的强大免疫反应有利于对抗Omicron变体的宿主传播,这种能力应该对管理高传染性病毒有用。
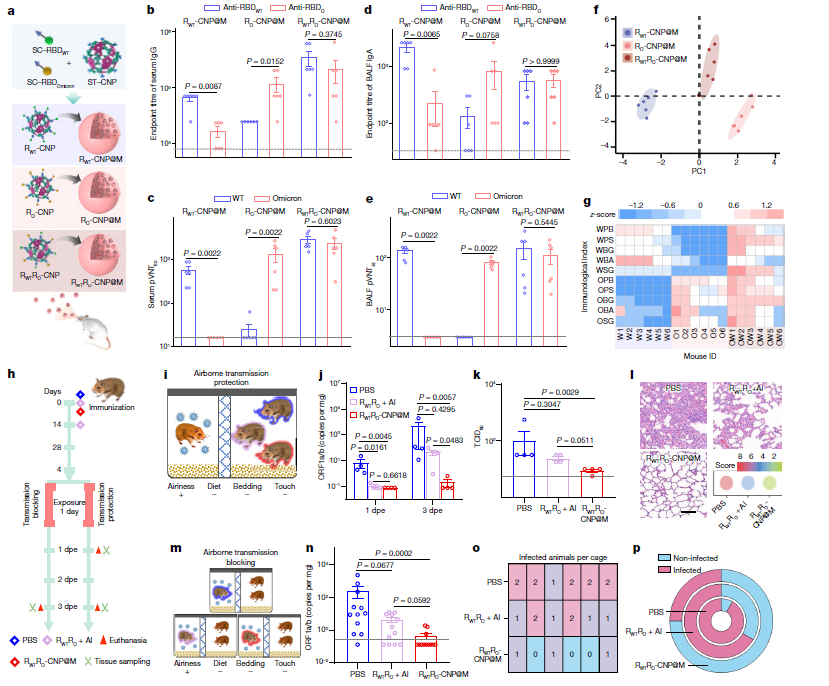
什么是ImmuHub®技术?
关于艾沐蒽
杭州艾沐蒽生物科技有限公司成立于2016年,是国际前沿的专注于免疫驱动医学技术的国家高新技术企业。创始人团队来自美国芝加哥大学,在2010年开始使用免疫组基因高通量测序技术开展各种疾病相关研究,于2016年通过自主研发,全国率先推出NGS-MRD血液肿瘤微小残留病(MRD)检测Seq-MRD®,并授权泛生子(纳斯达克代码:GTH)使用。同时,公司拥有Immun-Traq®肿瘤治疗伴随诊断、Immun-Cheq® |T细胞免疫测评以及ImmuHub®免疫组测序科研服务产品,并布局有基于AI机器学习算法的T-classifier®肿瘤早筛、单细胞测序、TCR-T和抗体发现等平台管线。目前为止发表了数十篇论文,其中包括:Nature(IF:65), Signal Transduction and Targeted Therapy(IF:40), Cellular and Molecular Immunology(IF:24), Nature Communications (IF:17)等多篇高分杂志。公司构建几十项发明专利和软件著作权为核心的自主知识产权体系,为医院临床、生命科学研究、新药开发等提供解决方案和产品。艾沐蒽专注于通过解码适应性免疫系统来改变疾病的诊断和治疗,并致力于推进免疫驱动医学领域发展。
杭州艾沐蒽生物科技有限公司
ImmunoDiagnostics | ImmunoMonitoring
免疫诊断 | 免疫监控
专注于免疫组高通量测序

长按关注艾沐蒽生物
ImmuHub | Seq-MRD | Seq-SHM | Immun-Traq| Immun-Cheq
Web:www.immuquad.com
Email:Contact@immuquad.com
Tel:0571-81061561
地址:杭州市上城区石桥路196号浙江省农创园4号楼1层

