依据Ig NGS技术的MRD进展水平调整MM治疗决
发布时间:2025-02-24 15:10 | 点击次数:752
多发性骨髓瘤是一种常见的血液系统恶性肿瘤,其治疗目标是尽可能延长患者的无病生存期和总生存期。近年来,随着医学技术的飞速发展,多发性骨髓瘤(MM)的治疗取得了显著进步。特别是在新诊断多发性骨髓瘤(NDMM)患者中,四联疗法(QUAD)结合自体干细胞移植(ASCT)已成为标准治疗方案之一。然而,随着越来越多的患者达到严格的完全缓解(sCR),传统基于血清和尿液副蛋白的评估标准已不足以满足精准医疗的需求。此时,微小残留病(MRD)检测的重要性愈发突显。
微小残留病 (Minimal Residual Disease, MRD) 是指白血病/淋巴瘤/骨髓瘤患者经治疗缓释后,体内仍残留少量癌细胞的状态,最终可能会引起疾病复发。它是衡量治疗效果和预测疾病复发的重要指标。在NDMM患者中,MRD阴性状态通常与更长的无进展生存期(PFS)和总生存期(OS)相关。此外,在近期发布的《多发性骨髓瘤疗效评估与微小残留病监测中国指南(2024年版)》中也强调了NGS技术在MM MRD检测中的优势和作用。
国际骨髓瘤工作组(IMWG)制定了统一的响应和进展标准,但这些标准主要依赖于血清和尿液中的副蛋白水平。随着治疗的进步,许多患者达到了无法检测到副蛋白的状态,因此需要更敏感的工具来评估疾病的动态变化。下一代测序(NGS)技术的应用使MRD检测成为可能,并逐渐成为临床试验和日常实践中的关键指标。

最近发表在《Blood Cancer Journal》(IF:12.9)上的一项研究分析了216名NDMM患者的MRD数据。这些患者接受了包含达雷妥尤单抗、卡非佐米、来那度胺和地塞米松(Dara-KRd)的四联疗法或类似的四联方案(Dara-VRd),随后进行自体干细胞移植(ASCT)。研究通过免疫组NGS技术连续监测患者的MRD状态,揭示了MRD进展(MRD-P)对多发性骨髓瘤的临床意义。
MRD-P被任意定义为MRD数值最低点基础上增加至少1个对数级(log10)以上。对于MRD<10^-6的患者,增加1个对数级(log10)之后,即MRD达到≥10^-5时,即认为是MRD-P。
研究结果
1.MRD阴性率显著提升
研究显示,在接受QUAD+ASCT治疗的患者中,78%的患者在10⁻⁵阈值下达到MRD阴性,而68%的患者在更严格的10⁻⁶阈值下也实现了MRD阴性。这一结果表明,QUAD+ASCT方案在清除恶性克隆方面具有显著效果。
2.MRD进展的时间特征
从治疗开始到MRD进展(MRD-P)的中位时间为24.4个月。在19位患者发生MRD-P时,大多数患者(63%)处于观察状态,少数仍在接受治疗。其中17例(89%)患者的最近一次的MRD评估值<10⁻⁵,其中10例(53%)患者的MRD < 10⁻⁶。且而在MRD-P后,53%的患者改变了治疗方案,其中9人转为使用含抗CD38单克隆抗体的方案。这提示,即使在达到深度缓解后,持续监测MRD状态仍然非常重要。
此外,从MRD进展(MRD-P)到国际骨髓瘤工作组(IMWG)定义的经典疾病进展(PD)的中位时间为10.1个月。这一发现表明,MRD-P可以作为经典PD的一个早期预警信号,有助于及时调整治疗策略。
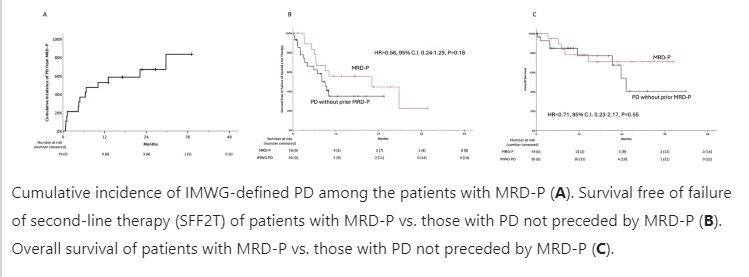
3.生存结局分析
研究通过对比生存结局,结果显示MRD-P患者的1年无第二线治疗失败生存率(SFF2T)为56%,而经典PD患者为35%;MRD-P患者的2年总生存率(OS)为78%,而经典PD患者为54%。尽管样本量较小且存在一定的偏倚,但研究结果表明,MRD进展与经典的IMWG定义的疾病进展具有相似的预后意义。
小 结
这项研究首次在四药联合疗法加ASCT的背景下探讨了MRD进展的意义。研究结果表明,在现代多发性骨髓瘤治疗中,MRD的上升可能是疾病活跃且难以被控制的可靠指标。与以往的研究相比,本研究中接受四药联合疗法的患者,MRD进展后到PD的时间更短,预后更差。这表明,四药联合疗法虽然显著提高了MRD阴性的比例,但对于那些即使在这种强效治疗下仍出现MRD-P的患者,可能预示着疾病更具侵袭性和耐药性。因此当患者出现MRD-P时,应及时调整治疗方案以此延缓经典PD的发生并改善生存结局。
总之,在QUAD+ASCT治疗背景下,MRD-P具有重要的临床意义。MRD-P是经典疾病进展(PD)的重要早期信号,而及时调整治疗方案可以有效延缓疾病恶化并提升患者生存率。艾沐蒽的Seq-MRD®技术以其极高的灵敏度和特异性,能够检测到10⁻⁶水平的残留恶性浆细胞克隆,为多发性骨髓瘤患者的治疗带来更精准、更个性化的医疗解决方案。
参考文献:Costa, L.J., Medvedova, E., Dhakal, B. et al. Implications of isolated MRD progression in newly diagnosed multiple myeloma treated with quadruplet therapy. Blood Cancer J. 15, 13 (2025).

Seq-MRD®相关认证及荣誉
1.获得欧盟CE资质认证
Seq-MRD®获得欧盟CE资质(注册号:DE/CA20/01-IVD-Luxuslebenswelt-190/22),获批的是人淋巴B细胞微小残留病基因检测试剂盒(可逆末端终止测序法)。

2.获得三项发明专利
艾沐蒽推出的Seq-MRD®血液癌症MRD检测是最早批实现商业化的产品,自2016年研发专利技术至今,艾沐蒽Seq-MRD®已经获得3项国家发明专利:
[1]“一种应用于高通量测序检测T细胞白血病微小残留病的引物组合及试剂盒”(专 利 号: 2016 11204857.0,授权公告号:CN 106957906 B)
[2]“一种检测微小残留病MRD的试剂盒”(专 利 号: 2018 1 1550133.0,授权公告号: CN 109652518 B)
[3]“一种检测微小残留病MRD的方法”(专 利 号: 2018 1 1549203.0,授权公告号: CN 109680062 B)

3.获得相关软件著作
艾沐蒽拥有自主研发的生信分析平台,艾沐蒽Seq-MRD® 已经获得3项国家计算机软件著作:
[1]“免疫组库MRD检测自动化报告系统[简称ImmuReport] V1.0”(登记号:2019SR0916207)
[2]“Seq-MRD检测自动化分析系统(DiscTermite)[简称:DiscTermite]0.4.6“(登记号:2019SR1131517)
[3]“基于免疫组库二代测序的微小残留病(MRD)检测数据处理系统”(登记号:2020SR0507594)

4.获得ISO双标体系认证
艾沐蒽生物成功通过ISO27001信息安全管理体系认证和ISO9001质量管理体系认证。

5.获得荣誉证书
艾沐蒽申报的“免疫组TCR/Ig高通量测序技术/血液肿瘤微小残留病(MRD)检测/Seq-MRD®”因其创新性、前沿性、市场实用性荣获“2022年度CCTB中国肿瘤标志物产业创新大会创新技术/产品评选”项目二等奖。

6.获批IVD一类证
2023年获批了【全血/骨髓基因组DNA提取试剂盒】(离心吸附柱法)备案编号:浙杭械备20230798 ,试剂盒分别适用于人外周血、骨髓样本的核酸的提取。
发表相关文献
Seq-MRD®发表相关文献
1、Huang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H. Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. Bone Marrow Transplant. 2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.




获得国际市场认可
2023年DelveInsight公司发布的MRD国际市场研究报告中,艾沐蒽/Seq-MRD®是中国独一一家公司/产品进入国际调研市场报告。DelveInsight是一家位于前列的医疗保健市场研究和商业咨询公司,以其现成的联合市场研究报告以及为医疗保健行业的公司提供的定制解决方案而闻名。



ImmunoDiagnostics | ImmunoMonitoring
免疫诊断 | 免疫监控
专注于免疫组高通量测序
ImmuHub | Seq-MRD | Immun-Traq
| Immun-Cheq | T-Classifier |TCR-T

