艾沐蒽科研服务平台:基于TCR的新抗原预测,解锁个体化免疫治疗的核心密码
发布时间:2025-06-20 18:05 | 点击次数:10280
近年来免疫疗法蓬勃发展,成为肿瘤治疗的一个重要手段。它旨在激活人体免疫系统,让其精准识别并摧毁肿瘤细胞。但目前市场上的免疫治疗效果有限,原因在于缺乏肿瘤特异性,无法精准识别肿瘤细胞,导致对正常细胞的误伤。
艾沐蒽基于全球先进的免疫组库分析平台,推出基于TCR的新抗原预测及验证服务,探索新型治疗靶点,解锁个体化免疫治疗的核心密码。
解码精准免疫治疗-- 基于TCR的新癌抗原预测
新癌抗原(Neo-antigen),就是特属个体肿瘤的基因翻译蛋白以抗原形式呈递在癌细胞或抗原呈递细胞表面,能被免疫系统识别,从而精准区分正常组织与癌组织。
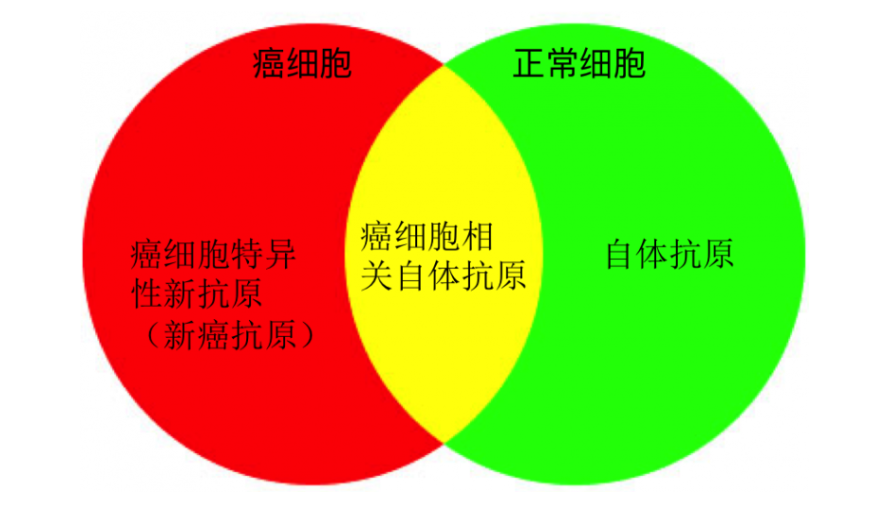
通过肿瘤细胞基因测序,找到患者特有的癌携基因,结合HLA分型进行免疫呈递亲和力预测,筛选出由癌携基因编码的癌抗原,即新癌抗原。配合TCR基因测序,能找出肿瘤突变与免疫系统之间的重要关系,更有助于制定个性化的癌症免疫治疗方案。
基于TCR的新抗原预测及验证服务流程如下:
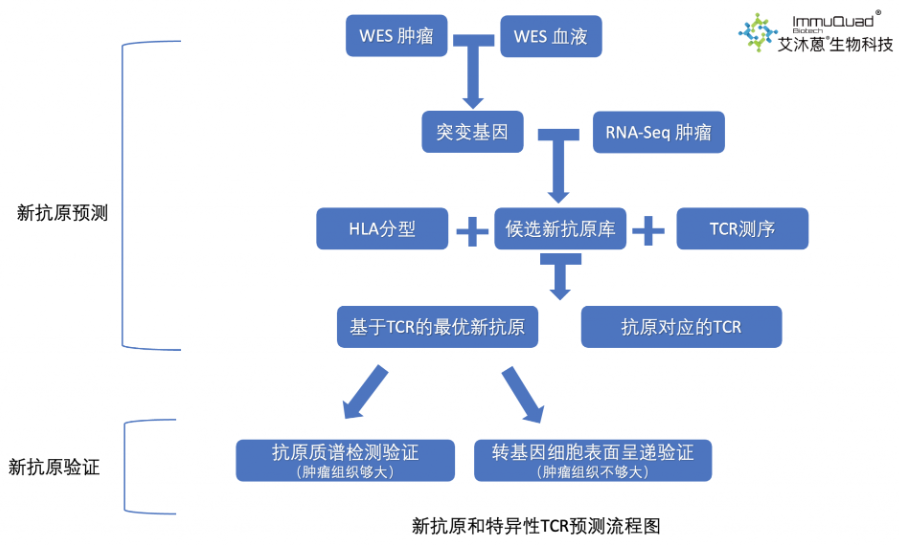
新抗原预测应用
-
通过预测肿瘤中的特异性新抗原,可以设计个性化的疫苗,激发患者体内免疫系统对肿瘤细胞的特异性免疫反应。
-
新抗原还可以用于过继性T细胞治疗(如CAR-T、TCR-T细胞疗法等),通过识别和筛选能够识别新抗原的TCR,可以设计出针对特定新抗原的T细胞,增强对肿瘤的杀伤能力。
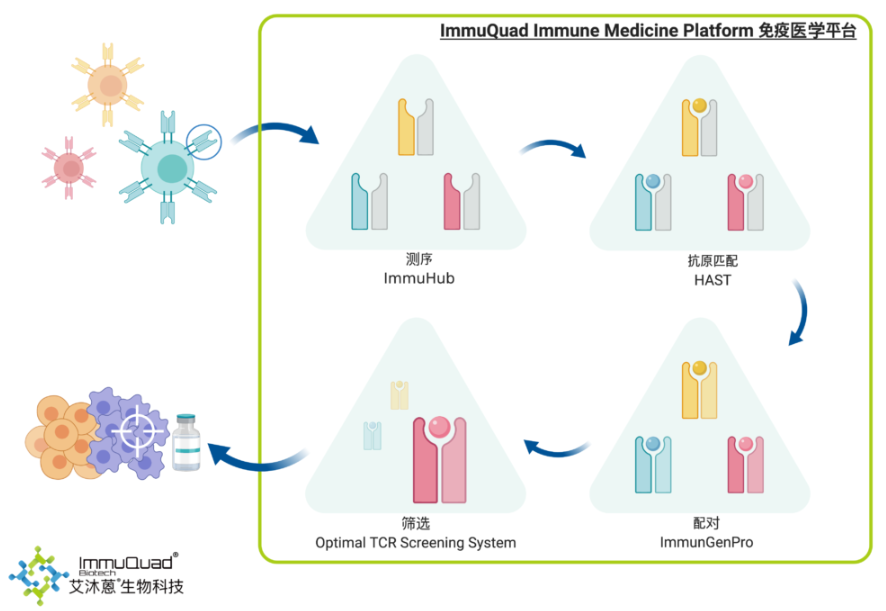
文献分享
2025年1月《Nature Medicine》发布了一项个体化mRNA新抗原疫苗Autogene cevumeran(iNeST)的I期临床研究进展,该研究在晚期实体瘤患者中展现出显著的安全性和免疫原性。这代表着癌症疫苗从"通用型"迈向"个体化精准治疗"的新纪元。

首先获取患者的肿瘤组织样本和外周血样本,进行高通量测序,识别体细胞突变,通过生物信息学分析预测潜在的 T 细胞免疫诱导新抗原,综合考虑 HLA I 类和 II 类分子的结合亲和力、转录表达水平等因素,最终选择最多20个新抗原作为iNeST的靶点。这些新抗原随后被合成为多肽,并用于体外刺激试验,以激活患者自身的T细胞。
2.临床研究方案
入组213例晚期实体瘤患者,分为1a期iNeST单药治疗研究(n=30)和1b期iNeST联合阿替利珠单抗治疗研究(n=183)。评估安全性、耐受性、药代动力学、药效学、初步抗肿瘤活性和免疫原性。
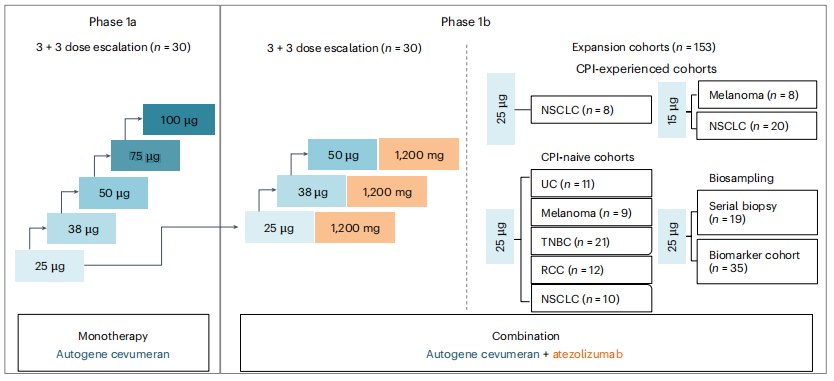
3.研究结果
-
安全性和耐受性
iNeST单药治疗的不良事件(TRAEs)主要为输液相关反应、细胞因子释放综合征(CRS)等,多为 1 - 2 级,可管理,1例出现 3 级剂量限制性毒性,治疗后恢复。联合治疗整体不良事件的类型和频率与阿替利珠单抗治疗一致,未观察到新的安全性信号。
-
免疫原性
71% 患者诱导出针对多种新抗原的特异性T细胞应答,运用pMHC多聚体技术分析这些特异性T细胞的动态变化,在疫苗接种后3周即可检测到特异性CD8+ T细胞响应,且可持续长达23个月。通过TCR测序技术发现70.07%的特异性T细胞为基线时未检测到的新生克隆(图h),肿瘤组织与外周血的TCR克隆呈现高度重叠,证实了疫苗诱导的T细胞具备肿瘤归巢能力(图i)。
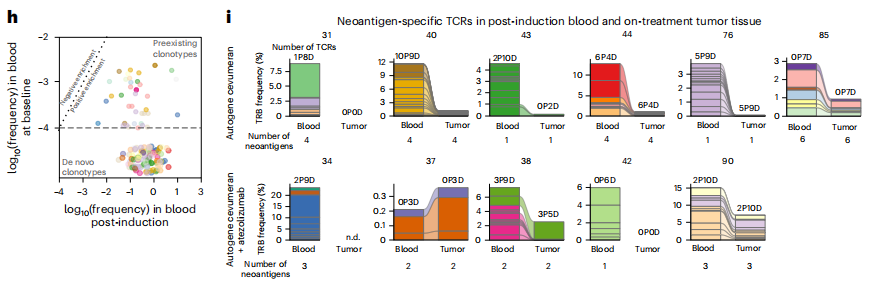
-
初步抗肿瘤活性
单药和联合治疗均观察到临床活性,如完全缓解和部分缓解,不同肿瘤类型的客观缓解率存在差异。患者基线特征和生物标志物与疾病进展相关。
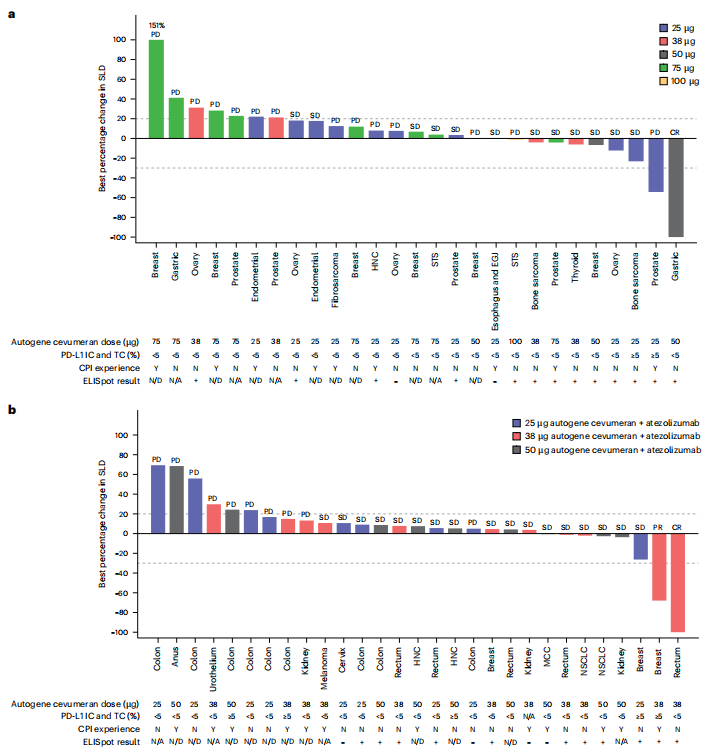
4.研究结论
个体化新抗原疫苗iNeST在晚期实体瘤患者中具有可行性和耐受性,免疫原性良好,可诱导强烈的 T 细胞反应,支持其在早期治疗阶段的进一步研究,以改善患者预后。
参考文献:Lopez, J., Powles, T., Braiteh, F. et al. Autogene cevumeran with or without atezolizumab in advanced solid tumors: a phase 1 trial. Nat Med31 , 152–164 (2025).
艾沐蒽生物科技,作为精准医疗的先行者,将继续致力于推动个性化免疫疗法的发展,为患者提供更多希望和选择。我们期待与更多的科研机构、企业合作,共同探索精准免疫治疗的无限可能!


