96分顶刊研究:96分顶刊研究:NGS-MRD阴性骨髓瘤患者,竟能跳过这个 “必做” 治疗?
发布时间:2025-07-24 15:32 | 点击次数:514
多发性骨髓瘤(MM)是一种浆细胞恶性肿瘤,MRD是评估治疗效果和预测疾病进展的重要指标。目前,对于新诊断的多发性骨髓瘤患者(NDMM),标准治疗方案包括四药联合诱导治疗后进行自体干细胞移植(ASCT)。上一期我们分享了一篇文章,关于采用NGS MRD技术评估独立于诱导治疗的ASCT效应,建立ASCT前后的MRD轨迹,为开发新型T细胞疗法提供了关键基准。那对于诱导治疗后达到MRD阴性的患者来说ASCT是否仍是必选项?
这一期我们继续分享一篇关于MM MRD检测的高分文章,发表于The New England Journal of Medicine(IF:96.2)的一篇临床试验研究,剖析了ASCT对MRD阴性NDMM患者是否具有必要性以及串联ASCT对于高危患者的收益,探索基于NGS MRD结果个性化制定巩固治疗策略。

研究方法
这是一项开放标签、随机、III期临床试验,共纳入791名患者,其中757名完成了六周期的Isa-KRd(isatuximab, carfilzomib, lenalidomide, dexamethasone)诱导治疗。根据诱导治疗后的NGS MRD状态(cutoff=10^-5),患者被随机分配到不同的巩固治疗组,如下。以维持治疗前达到NGS MRD阴性(<10^-6)状态为主要终点。
-
分组1:MRD阴性(<10^-5)患者随机分配到ASCT组(接受ASCT后进行两周期Isa-KRd)或Isa-KRd组(接受六周期Isa-KRd)。
-
分组2:MRD阳性(大于10^-5)患者随机分配到串联ASCT组或单次ASCT组(接受ASCT后进行两周期Isa-KRd)。
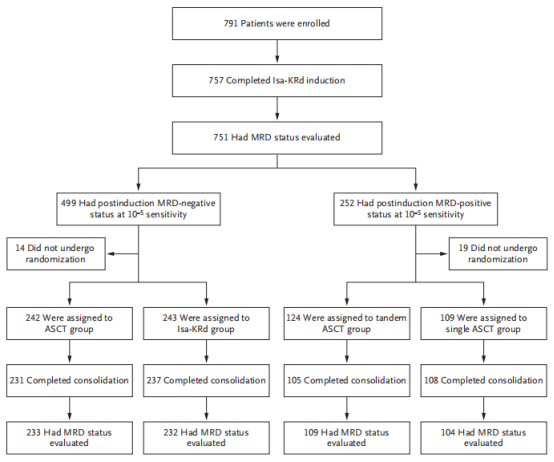
图1
研究结果
1.ASCT VS. Isa
在485名诱导治疗后MRD阴性的患者中,ASCT组和Isa-KRd组在维持治疗前达到10^-6敏感度的MRD阴性状态的比例分别为86%和84%(p=0.64)(图2A)。在巩固治疗阶段,ASCT组和Isa-KRd组分别有53例患者和42例患者转换为MRD阴性(<10^-6),分别有6例和10例患者MRD转阳(图2B)。
以上表明在MRD阴性患者中,ASCT与Isa-KRd相比,并未显著提高达到更高敏感度MRD阴性的比例。
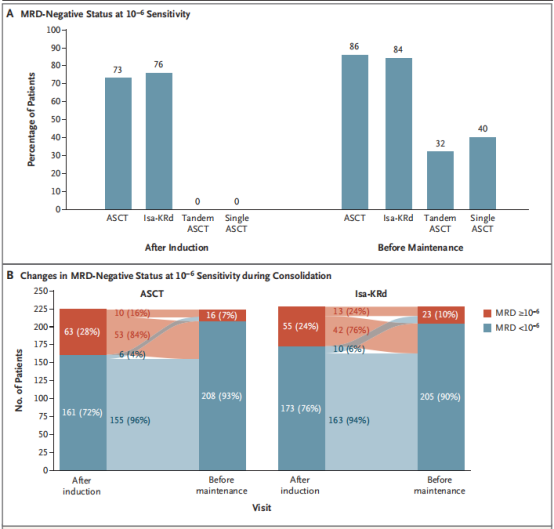
图2
2.串联ASCT VS. 单次ASCT
在233名诱导治疗后MRD阳性的患者中,串联ASCT组和单次ASCT组在维持治疗前达到10^-6敏感度的MRD阴性的比例分别为32%和40%(P=0.31)(图2A)。在维持治疗之前,串联ASCT组中有61%的患者达到了MRD阴性,单次ASCT组中这一比例为67%。
以上表明在MRD阳性患者中,串联ASCT与单次ASCT相比,并未显著提高达到更高敏感度MRD阴性的比例。
3.安全性
与诱导期相比,巩固期未出现新的安全性信号。不同分组的3级以上不良事件详见图3.
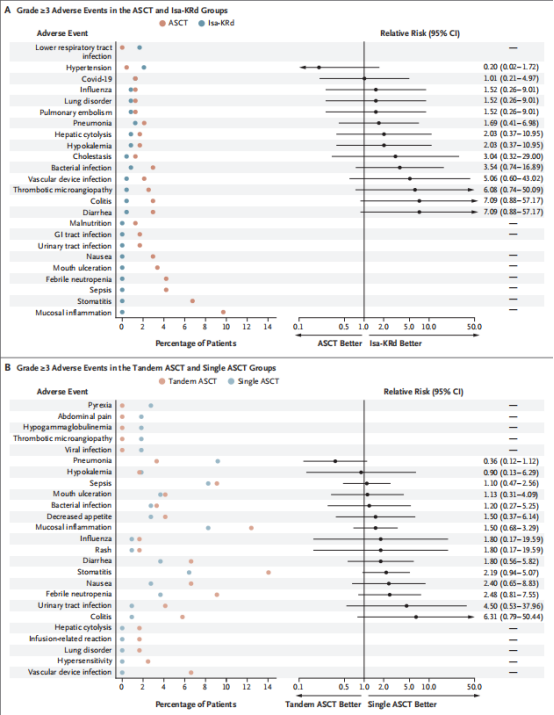
图3
研究结论
在诱导治疗后MRD阴性的患者中,ASCT与Isa-KRd相比,并未显著提高维持治疗前MRD阴性状态的比例;在诱导治疗后MRD阳性的患者中,串联ASCT与单次ASCT相比,也并未显著提高维持治疗前MRD阴性状态的比例。表明在有效的四药联合诱导治疗后,传统的ASCT和串联ASCT可能不再是所有患者的最佳选择,特别是在MRD阴性患者中。该研究为在NGS MRD的指导下制定MM个性化治疗策略提供了重要的数据支持。
参考文献:Perrot A, Lambert J, Hulin C, et al. Measurable Residual Disease-Guided Therapy in Newly Diagnosed Myeloma. N Engl J Med. Published online June 3, 2025. doi:10.1056/NEJMoa2505133
艾沐蒽专注于免疫组二代测序领域多年,是国内首家推出血液肿瘤NGS MRD检测产品Seq-MRD®的公司。Seq-MRD®适用于B/T系白血病、B/T系淋巴瘤、多发性骨髓瘤,能够帮助临床医生预测长期疗效、评估治疗效果、监测缓解状态以及监测早期复发。经过多年的积累和发展,Seq-MRD®在临床检测和科学研究上均取得不少成果,并获得国际市场认可。
Seq-MRD®相关认证及荣誉
1.获得欧盟CE资质认证
Seq-MRD®获得欧盟CE资质(注册号:DE/CA20/01-IVD-Luxuslebenswelt-190/22),获批的是人淋巴B细胞微小残留病基因检测试剂盒(可逆末端终止测序法)。

2.获得三项发明专利
艾沐蒽推出的Seq-MRD®血液癌症MRD检测是最早批实现商业化的产品,自2016年研发专利技术至今,艾沐蒽Seq-MRD®已经获得3项国家发明专利:
[1]“一种应用于高通量测序检测T细胞白血病微小残留病的引物组合及试剂盒”(专 利 号: 2016 11204857.0,授权公告号:CN 106957906 B)
[2]“一种检测微小残留病MRD的试剂盒”(专 利 号: 2018 1 1550133.0,授权公告号: CN 109652518 B)
[3]“一种检测微小残留病MRD的方法”(专 利 号: 2018 1 1549203.0,授权公告号: CN 109680062 B)

3.获得相关软件著作
艾沐蒽拥有自主研发的生信分析平台,艾沐蒽Seq-MRD® 已经获得3项国家计算机软件著作:
[1]“免疫组库MRD检测自动化报告系统[简称ImmuReport] V1.0”(登记号:2019SR0916207)
[2]“Seq-MRD检测自动化分析系统(DiscTermite)[简称:DiscTermite]0.4.6“(登记号:2019SR1131517)
[3]“基于免疫组库二代测序的微小残留病(MRD)检测数据处理系统”(登记号:2020SR0507594)

4.获得ISO双标体系认证
艾沐蒽生物成功通过ISO27001信息安全管理体系认证和ISO9001质量管理体系认证。

5.获得荣誉证书
艾沐蒽申报的“免疫组TCR/Ig高通量测序技术/血液肿瘤微小残留病(MRD)检测/Seq-MRD®”因其创新性、前沿性、市场实用性荣获“2022年度CCTB中国肿瘤标志物产业创新大会创新技术/产品评选”项目二等奖。

6.获批IVD一类证
2023年获批了【全血/骨髓基因组DNA提取试剂盒】(离心吸附柱法)备案编号:浙杭械备20230798 ,试剂盒分别适用于人外周血、骨髓样本的核酸的提取。
发表相关文献
Seq-MRD®发表相关文献
1、Huang Y, Zhao H, Shao M, Zhou L, Li X, Wei G, Wu W, Cui J, Chang AH, Sun T, Hu Y, Huang H. Predictive value of next-generation sequencing-based minimal residual disease after CAR-T cell therapy. Bone Marrow Transplant. 2022 Jun 1. doi: 10.1038/s41409-022-01699-2. Epub ahead of print. PMID: 35650329.




获得国际市场认可
2023年DelveInsight公司发布的MRD国际市场研究报告中,艾沐蒽/Seq-MRD®是中国独一一家公司/产品进入国际调研市场报告。DelveInsight是一家位于前列的医疗保健市场研究和商业咨询公司,以其现成的联合市场研究报告以及为医疗保健行业的公司提供的定制解决方案而闻名。



