2025诺奖得主的早年“伏笔”:TCR 测序如何揭开自身免疫病的 “克隆密码”?
发布时间:2025-11-06 17:13 | 点击次数:364
当 2025 年诺贝尔生理学或医学奖授予 "外周免疫耐受" 研究的科学家时,很多人聚焦于调节性 T 细胞的 "免疫刹车" 作用。但鲜为人知的是,得主之一坂口志文团队早年关于 T 细胞受体(TCR)的研究 —— 尤其是TCR 测序技术的应用,为这一重大发现筑牢了根基。今天我们就通过团队于 2014 年发表在《Science》的文献,阐述TCR 测序如何帮科学家破解自身免疫病的 “克隆谜题”。

TCR的关键作用
作为 T 细胞表面的 “身份识别系统”,TCR 通过胚系基因 V (D) J 重排、核苷酸插入缺失,造就了 10¹⁵~10¹⁸ 种多样性,既能应对病原体,也可能错认自身蛋白引发疾病。但长期以来,科学家面临两大难题:一是致病T 细胞因识别普遍自身抗原,多在胸腺被清除,难以捕获;二是即便找到,也无法明确其TCR 克隆的真实构成 —— 而TCR 测序技术,恰恰为后者提供了破解工具。
捕获致病性TCR
团队先通过改造 TCR 信号通路,让致病 T 细胞逃避胸腺清除,再借助TCR 高通量测序,揭开了致病 T 细胞的 “群体真相”:
他们对 SKG 关节炎小鼠关节浸润的 CD4⁺T 细胞做 Vβ 家族测序(用 MiTCR 软件分析),发现致病 T 细胞是高度多克隆的 ——Vβ6⁺CD4⁺T 细胞的 CDR3 序列几乎无共通性(Fig 1),打破了 “致病 T 细胞为单克隆群体” 的推测;
进一步对单个关节浸润 T 细胞做 TCR 克隆测序,成功分离出致病 TCR 克隆 “7-39”,并通过测序验证:在不同患病小鼠关节中,均存在携带 7-39 样 Vβ CDR3 序列的 T 细胞,证实该克隆是关节炎的 “关键元凶”(Fig 2)。
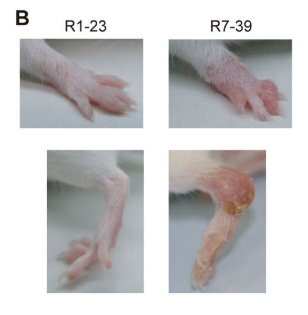
Fig 2
更关键的是,测序助力锁定了攻击目标:团队通过 “TCR 克隆 - 抗原匹配”,结合质谱鉴定,发现7-39 TCR 特异性识别普遍表达的核糖体蛋白 RPL23a。这一突破,正是基于TCR 测序对 “单一致病克隆” 的精准追踪 —— 若没有测序,根本无法从海量 T 细胞中定位到这一低丰度的致病克隆。
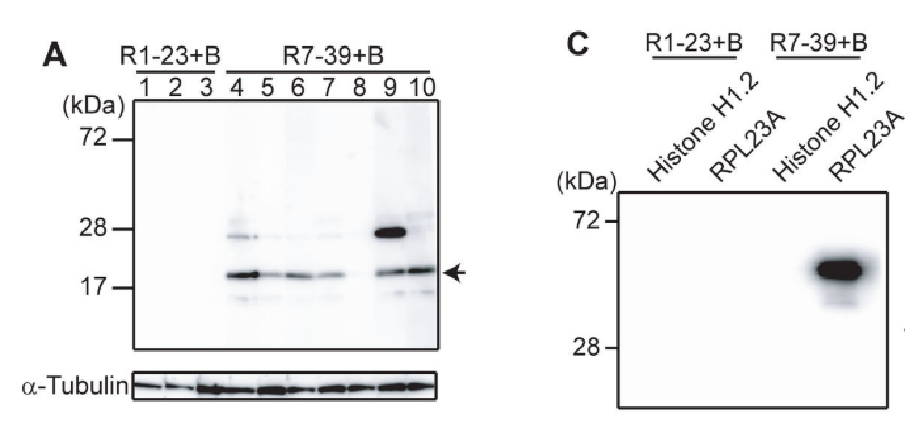
Fig 3
理论的最后一步是回归人类疾病。团队在RA 患者中进行了验证:
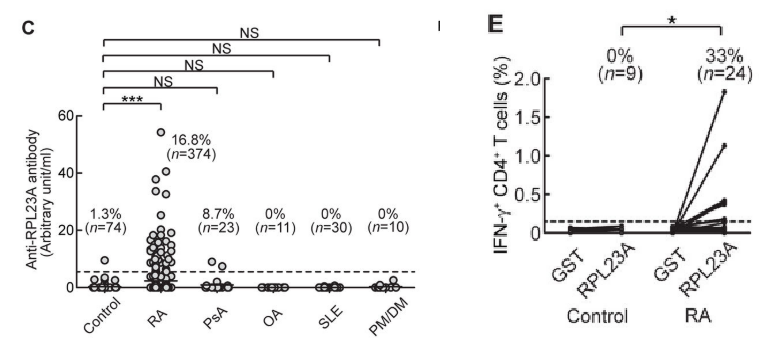
Fig 4 (GST:谷胱甘肽酶)
TCR 测序如何推动免疫耐受研究
在文献方法学中,团队优化的TCR 测序 + 克隆验证技术,是破解免疫耐受机制的核心工具:
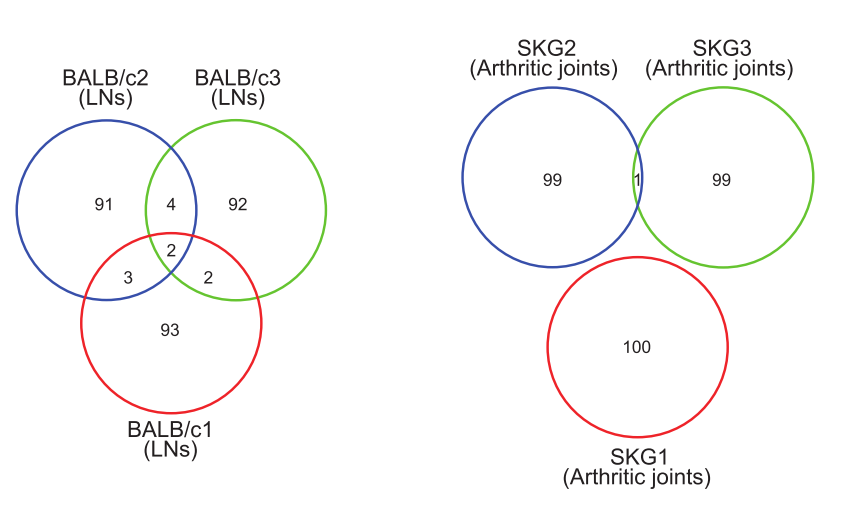
揭示TCR 库偏移:对比正常BALB/c 小鼠与 SKG 关节炎小鼠的 TCR 库,发现后者存在独特 CDR3 序列扩增(如 7-39 样序列),证实自身免疫病中 “耐受失效导致致病 TCR 克隆累积”;明确发病链条:通过测序确认RPL23A-MHC-TCR 的特异性结合 —— 当RPL23A 异常提呈时,其特异性 TCR 被激活,攻击关节滑膜。这一链条的阐明,让调节性T 细胞的 “刹车作用” 有了明确靶点:诺奖成果中调节性 T 细胞的核心功能,正是抑制这类经测序鉴定的致病性TCR 克隆。
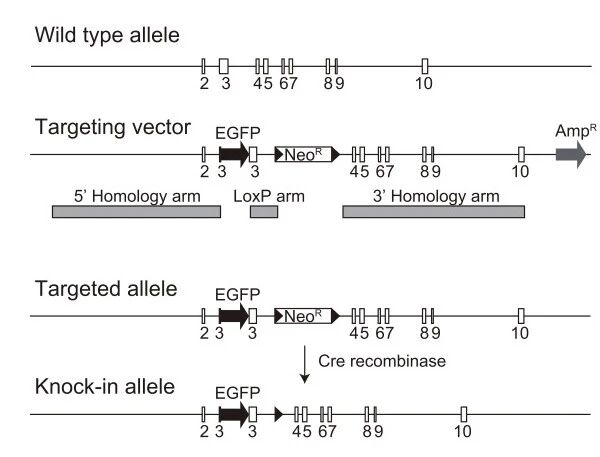
Fig 5
启示与展望
如今,TCR 测序已从基础研究走向临床,在自身免疫病的精准防控中展现出明确价值,每一项应用都与致病 TCR 克隆的测序解析息息相关,如:
诊断标志物:检测患者体内7-39 样 TCR 克隆丰度,可早于关节损伤信号诊断RA;
诺奖委员会评价 “外周免疫耐受的发现离不开T 细胞识别机制的理解”,而 TCR 测序正是这一理解的“显微镜”—— 它让隐形的致病TCR 克隆显形,让免疫耐受的研究从 “宏观现象” 走向 “微观精准”,也为自身免疫病治疗打开了 “靶向时代” 的大门。

什么是ImmuHub®技术?
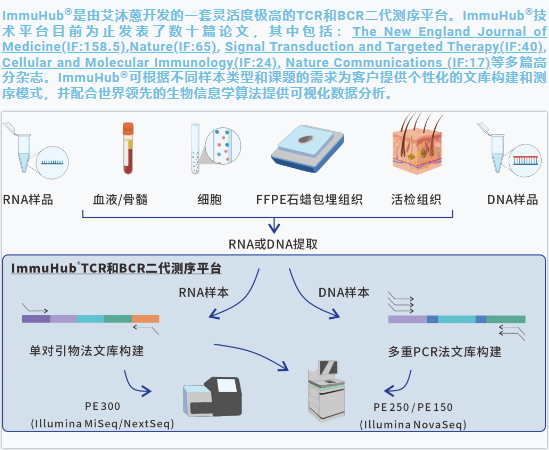
ImmuHub®部分科研方向

ImmuHub®适用基因座
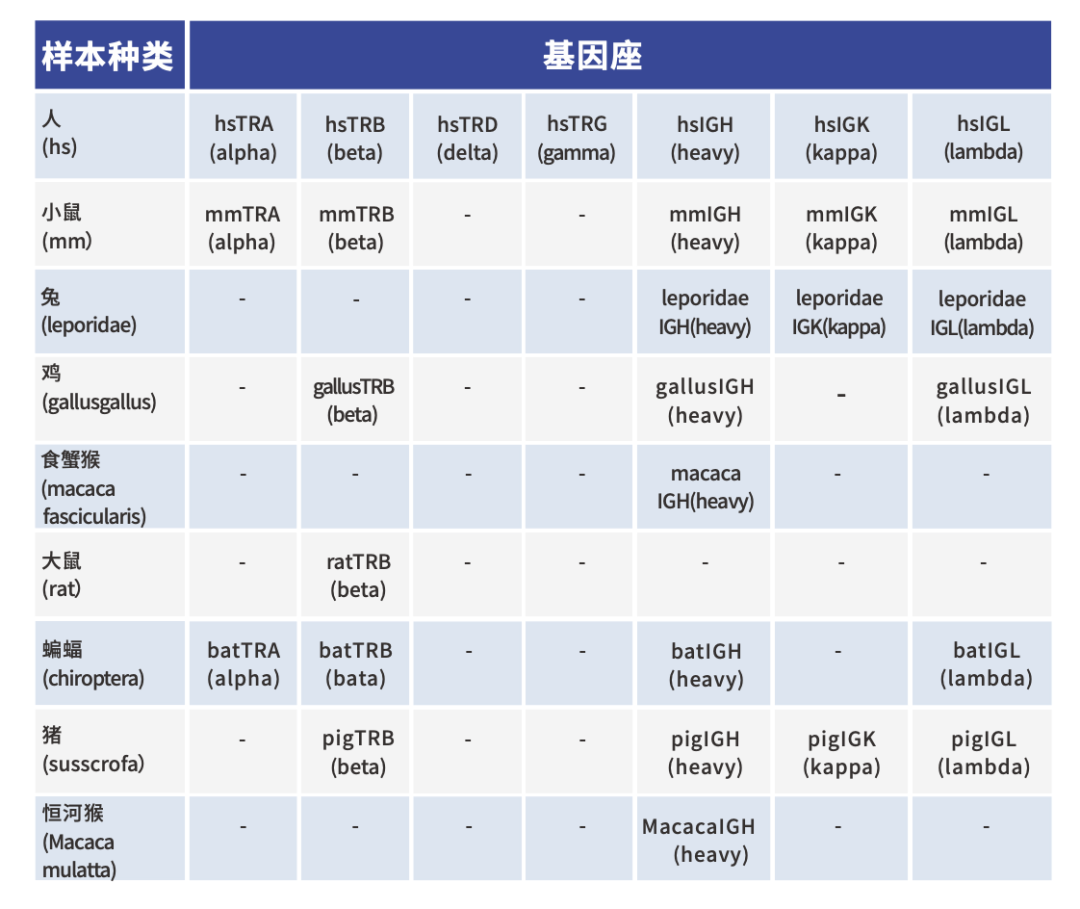
部分数据分析结果展示